
Actualidad Cientifica
Revista 623
Un análisis de sangre para diagnosticar depresión

Investigadores del Conicet han demostrado la conexión entre la activación inmunológica y los trastornos del estado de ánimo. Evaluaron en sangre las células de la inmunidad innata y adaptativa, y lograron discriminar entre pacientes con depresión y controles sanos con una precisión del 83.8%. Estos hallazgos serían clave para aplicar nuevas estrategias terapéuticas. Restan futuros estudios para llevar el análisis a la práctica clínica.
Por Ana M. Pertierra
La depresión es una de las enfermedades mentales más frecuentes en el mundo. Se estima que más de 300 millones de personas la padecen, y en Argentina, se calcula que alrededor del 5,7 por ciento de la población sufre algún trastorno del estado de ánimo. El papel del sistema inmunológico en su patogénesis es cada vez más reconocido, sin embargo faltaba una comprensión integral sobre la participación de las células inmunes innatas y adaptativas.
Así fue que un equipo de investigación, liderado por los Dres. Federico Daray y Andrea Errasti, especialistas del CONICET en el Instituto de Farmacología de la UBA, decidió analizar esa relación para ver si era posible identificar a los pacientes con depresión a través del análisis de la respuesta inmune en sangre. Realizaron un estudio multicéntrico de casos y controles con 121 participantes emparejados por sexo y edad, 39 tenían un episodio depresivo mayor, 40 pacientes en remisión y 42 controles sanos a los que les analizaron sus perfiles inmunológicos.
En muestras de sangre determinaron el recuento celular completo y los subtipos de monocitos y poblaciones de células T de linfocitos mediante citometría de flujo. Además, de medir un panel de citocinas, quimiocinas y factores neurotróficos en el plasma. Uno de los hallazgos más importantes del estudio fue que los pacientes con depresión, aun en remisión, exhibían un comportamiento alterado de su inmunidad innata y adaptativa.
En el Laboratorio de Inmunofarmacología del Instituto de Farmacología de la UBA trabajan en líneas de investigación centradas en entender la contribución del sistema inmune innato y los mecanismos patogénicos subyacentes de enfermedades con componente inflamatorio crónico y/o autoinmune. Los proyectos del laboratorio están enmarcados en una estrecha colaboración que aúnan los esfuerzos desde la clínica y la ciencia experimental básica.
El estudio se publicó en la revista Translational Psychiatry (https://www.nature.com/articles/s41398-024-02902-2)
FABAinforma se comunicó con la Dra. Andrea Emilse Errasti, Investigadora Independiente del CONICET, Prof. Reg. Adjunta 3º Cátedra de Farmacología de la Facultad de Medicina de la UBA, Directora Interina del Instituto de Farmacología de la Facultad de Medicina, UBA y una de las autoras del trabajo.

Dra. Andrea Errasti, investigadora independiente del CONICETen el Instituto de Farmacología de la UBA
Ya había evidencia de la relación entre la depresión y el funcionamiento del sistema inmunológico. ¿De qué modo se relacionan?
En las últimas décadas, se ha profundizado nuestro conocimiento sobre el sistema inmune más allá de su papel fundamental en la defensa contra infecciones por agentes patógenos. Se ha demostrado que el sistema inmune participa de tareas como la reparación tisular, la defensa antitumoral, el metabolismo, y más recientemente, su influencia sobre el comportamiento o estados del ánimo, como la depresión. En los últimos años, revisiones sistemáticas y meta-análisis, han demostrado una asociación entre la depresión y niveles elevados de citoquinas pro-inflamatorias en plasma, como la IL-6, IL-1β y TNF-α, además de la proteína C-reactiva (PCR). Aunque el cerebro se considera tradicionalmente un órgano inmunológicamente privilegiado, condiciones de estrés o inflamación pueden aumentar la permeabilidad de la barrera hemato- encefálica, permitiendo la entrada de estas citoquinas inflamatorias.
Estas citoquinas pueden activar la microglía, macrófagos residentes del sistema nervioso central, promoviendo la neuroinflamación. Además, el estrés psicosocial puede activar vías simpáticas eferentes, estimulando la producción y liberación de monocitos en la médula ósea que, a su vez salen a periferia y producen más citoquinas pro-inflamatorias. En modelos animales, la inducción de inflamación mediante lipopolisacáridos (LPS) o situaciones de estrés y aislamiento ha demostrado comportamientos similares a la depresión, reforzando la conexión entre la activación inmunológica y los trastornos del estado de ánimo.
¿Qué repercusión ha tenido la publicación de este estudio, que involucra directamente el sistema inmune con un estado de salud mental como la depresión mayor, entre la comunidad científica?
La comunidad científica ha mostrado un creciente interés y aceptación respecto al papel del sistema inmunológico en trastornos del estado de ánimo como la depresión. Si bien es prematuro saber cuál será el alcance de nuestra publicación, entendemos que es un claro aporte para sustentar que al menos un grupo de pacientes exhiben claramente que su sistema inmune a nivel de ciertas citoquinas y células de la sangre como los monocitos y los linfocitos T CD4, se encuentra alterado hacia un perfil inflamatorio. Esto obliga a repensar estrategias terapéuticas. Hoy en día, con la terapéutica actual se logra mejoría en solo un tercio de los pacientes, pero es importante vislumbrar que los mismos podrían beneficiarse de una terapéutica que contemple su estado inflamatorio.
¿Por qué se plantearon la evaluación de estos parámetros de la inmunidad mediante análisis de sangre en esta patología?
Consideramos que la sangre puede darnos información relevante acerca del estado inflamatorio del paciente, incluso para patologías del sistema nervioso central. La mayoría de los estudios en depresión se han focalizado en medir factores solubles, como las citoquinas y la PCR, en plasma. En nuestro equipo de trabajo, en la que logramos reunir áreas como médicos psiquiatras (liderados por el Dr. Federico Daray) e inmunólogos e inmuno- farmacólogos, (Dr. E. Antonio Carrera Silva y Dra. Andrea Errasti) pensamos que estudiar a las células de la inmunidad innata (monocitos) y de la inmunidad adaptativa (linfocitos T CD4), nos daría una información más robusta y estable para estudiar el perfil inflamatorio de los pacientes.
¿Cómo diseñaron el estudio? ¿Qué metodologías emplearon para el análisis y la obtención de los resultados?
Diseñamos un estudio multicéntrico y transversal que incluyó a 121 participantes divididos en tres grupos: voluntarios sanos, pacientes con diagnóstico de depresión en episodio activo y pacientes en remisión. El número de participantes se determinó para asegurar la solidez estadística en la evaluación de variables clínicas, de laboratorio e inmunológicas.
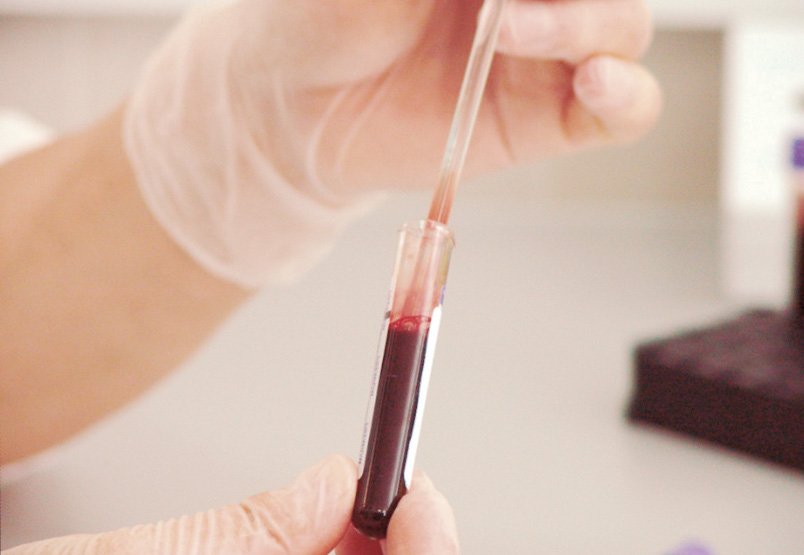
El diagnóstico clínico fue realizado por psiquiatras especializados y se recolectaron 20 mililitros de sangre de cada participante. Diez mililitros se destinaron a un hemograma completo, mientras que el resto se procesó en el Instituto de Farmacología de la Facultad de Medicina de la Universidad de Buenos Aires. En la Facultad realizamos una inmunofenotipificación detallada de monocitos y linfocitos T CD4 utilizando paneles de anticuerpos específicos y análisis por citometría de flujo. Además, medimos los niveles plasmáticos de PCR de alta sensibilidad mediante un método inmunoturbidimétrico y cuantificamos 16 citoquinas utilizando el sistema Legend Plex, también por citometría de flujo. Estos métodos combinados nos permitieron obtener un perfil inmunológico integral de los participantes y analizar diferencias significativas entre los grupos estudiados.
¿Cuáles son los resultados más novedosos y/o sorprendentes que obtuvieron?
Uno de los hallazgos más importantes es que los pacientes con depresión, aun en remisión, exhiben un comportamiento alterado de su inmunidad innata y adaptativa, reflejando un desbalance inflamatorio de bajo grado, pero persistente en el tiempo. Además, mediante técnicas de aprendizaje automático, identificamos un panel de biomarcadores que permitió discriminar entre pacientes con depresión y controles sanos con una precisión del 83.8%, superando nuestras expectativas iniciales y destacando la relevancia de los marcadores celulares en esta discriminación. Otro descubrimiento significativo fue la identificación de tres subgrupos inmunológicos distintos entre los pacientes con depresión a través de análisis de clústeres. Este hallazgo sugiere la posible existencia de diferentes fenotipos inmunológicos dentro de la depresión, lo que podría tener implicaciones importantes para la personalización de tratamientos en futuros estudios. Todo esto requiere de estudios de seguimiento (longitudinales) para ser corroborado.
¿De qué manera pueden estos resultados mejorar y/o modificar el tratamiento de la depresión?
Nuestros resultados sugieren que abordar la inflamación sistémica podría mejorar la eficacia de los tratamientos actuales para la depresión. Identificar a pacientes con un perfil inflamatorio específico permitiría integrar terapias antiinflamatorias o moduladoras del sistema inmunológico junto con los antidepresivos convencionales que actúan sobre neurotransmisores como la serotonina y la noradrenalina. Pensamos que este tipo de enfoques más personalizado podría aumentar la tasa de respuesta al tratamiento, especialmente en aquellos pacientes que no responden adecuadamente a las intervenciones estándar, y contribuir a desarrollar estrategias terapéuticas más efectivas y completas.
¿Cómo explican este comportamiento de las células inmunes en esta condición de enfermedad mental?
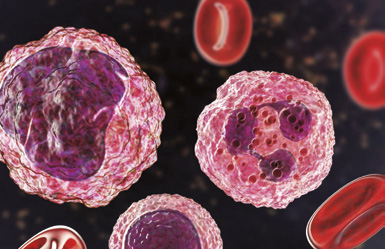
Los monocitos, son células de la inmunidad innata que muestran una gran plasticidad y pueden llegar a los tejidos de los diferentes órganos donde se pueden diferenciar a macrófagos y células dendríticas en respuesta a diferentes estímulos del microambiente tisular. El estrés psicosocial puede activar el sistema nervioso simpático, estimulando la liberación de monocitos desde la médula ósea hacia la circulación periférica, donde presentan niveles aumentados de activación en pacientes con depresión, según nuestros hallazgos. Estos monocitos activados pueden migrar al sistema nervioso central, actuando como “caballos de Troya” y promoviendo la neuroinflamación a través de la activación de la microglía y la producción adicional de citoquinas pro-inflamatorias, perpetuando así el ciclo inflamatorio asociado a la depresión. En cuanto a la inmunidad adaptativa, observamos que los linfocitos T CD4 en pacientes con depresión presentan signos de mayor activación y agotamiento, indicando una respuesta inmunológica crónicamente alterada. Otros estudios también reportan un aumento de la senescencia en estos linfocitos, lo que podría contribuir a una respuesta inmune menos efectiva y mantener el estado inflamatorio de bajo grado asociado con la depresión.
Las pruebas del laboratorio clínico participan en más de un 80% de los diagnósticos en distintas patologías y son clave para el seguimiento de los tratamientos. En este caso, los resultados de este estudio serían también un aporte fundamental a un diagnóstico diferencial. ¿Me podrá ampliar este concepto?
Consideramos que es un campo en crecimiento y si bien aún falta para trasladarlo a la práctica clínica, nos imaginamos que integrar nuestros hallazgos en prácticas de laboratorio clínico podría mejorar significativamente el diagnóstico y manejo de la depresión. La identificación de biomarcadores inmunológicos específicos en muestras de sangre permitiría, en principio, facilitar la detección de subtipos de depresión asociados con perfiles inflamatorios particulares. Este enfoque podría conducir a diagnósticos más precisos y a la implementación de tratamientos personalizados, optimizando la selección de terapias antiinflamatorias o inmunomoduladoras cuando sea apropiado. Aunque nuestros métodos actuales implican técnicas complejas como la citometría de flujo y paneles de múltiples citoquinas, trabajamos hacia la simplificación y estandarización de estas pruebas para su aplicación rutinaria en entornos clínicos, lo que eventualmente podría transformar la atención y el pronóstico de los pacientes con depresión.
