
SACT
Revista 622
Detección temprana de enfermedades hepáticas
Mejorar su identificación precoz es clave para minimizar la morbilidad y la mortalidad de la enfermedad hepática esteatótica asociada a la disfunción metabólica (MASLD), la esteatohepatitis asociada a la disfunción metabólica (MASH), la cirrosis, el carcinoma hepatocelular (CHC) y la enfermedad hepática terminal (ESLD).
En el próximo Congreso CALILAB 2024 que se llevará cabo en el Centro de Convenciones de CABA entre los días 6 al 8 de noviembre, se hará la presentación de los trabajos premiados por UNIVANTS, un programa de premios en Salud de Excelencia, en el que ADLM y Abbott premiaron a tres equipos por sus iniciativas de colaboración entre disciplinas combinadas con estrategias centradas en el paciente para mejorar los resultados de los mismos. En una nota, escrita por Kimberly Scott en el suplemento de Clinical Laboratory News comenta que “los equipos integrados de prestación de atención en todo el mundo están teniendo un impacto significativo y mensurable en los resultados de los pacientes al evolucionar, para ser más integrados, más centrados en el paciente y más ambiciosos en el uso de datos. Además, los profesionales del laboratorio clínico están aprovechando su posición única en la intersección de la tecnología y la atención al paciente para garantizar que las colaboraciones con médicos, administradores y otros profesionales de la salud puedan escalar para abordar los problemas de salud a nivel de la población”.
Entre las iniciativas premiadas que se consideraron, está la que estudió cómo mejorar la identificación temprana de enfermedades hepáticas, razón por la cual revisamos la literatura reciente y presentamos aquí algunos trabajos nuevos. Se sabe que la enfermedad hepática esteatótica asociada a la disfunción metabólica (MASLD) es una epidemia silenciosa que puede provocar esteatohepatitis asociada a la disfunción metabólica (MASH), cirrosis, carcinoma hepatocelular (CHC) y enfermedad hepática terminal (ESLD). Las investigaciones han demostrado que la identificación temprana de la enfermedad hepática puede minimizar la morbilidad y la mortalidad, pero esa identificación temprana a menudo puede ser difícil.
A continuación los trabajos seleccionados son:
- Ultrasonografía apoyada por inteligencia artificial: ¿puede ser la solución para el diagnóstico temprano y preciso de la enfermedad hepática esteatósica? Gabeta S, Rigopoulou EI, Dalekos GN. Eur J Intern Med. 2024; 125:41-43.
En diciembre pasado, un consenso Delphi de varias sociedades informó sobre la nueva nomenclatura y definiciones de la enfermedad del hígado graso. En consecuencia, los términos anteriores de enfermedad del hígado graso no alcohólico (NAFLD) y esteatohepatitis no alcohólica (NASH), que se basan en términos confusos excluyentes, así como en el posible uso de lenguaje estigmatizante, fueron reemplazados por enfermedad hepática esteatótica asociada a disfunción metabólica. (MASLD) y esteatohepatitis asociada a disfunción metabólica (MASH). Hoy en día, MASLD/MASH representan, con diferencia, la enfermedad hepática más común en todo el mundo, en paralelo con la creciente prevalencia de la obesidad y el síndrome metabólico (resistencia a la insulina y diabetes, hipertensión arterial, obesidad central y dislipidemia). MASLD se define como la presencia de esteatosis hepática, verificada mediante biopsia o imágenes, y se acompaña de al menos un factor cardiometabólico (sobrepeso u obesidad, intolerancia a la glucosa o diabetes tipo 2, hipertensión arterial, triglicéridos elevados y colesterol HDL bajo o tratamiento hipolipemiante).
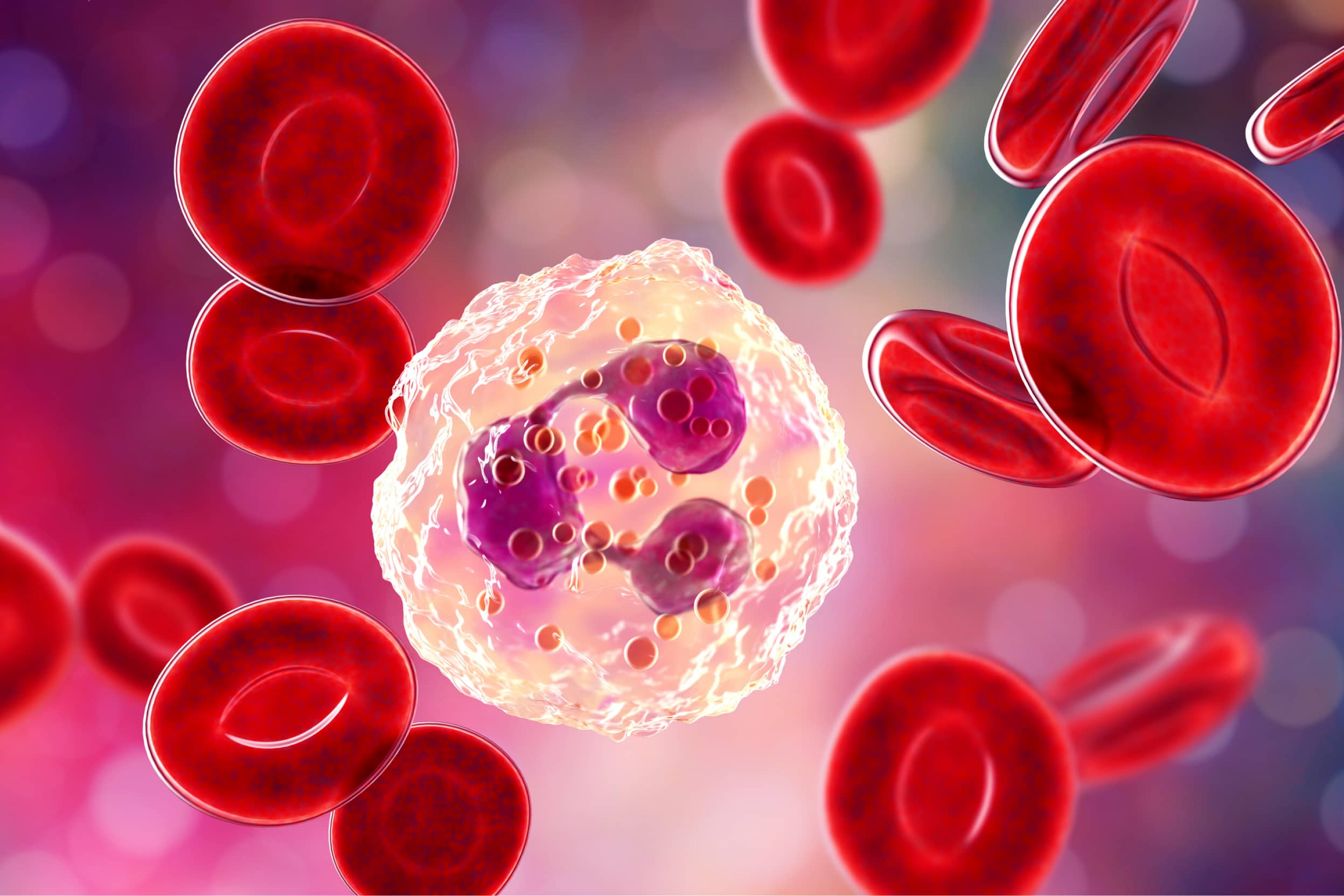
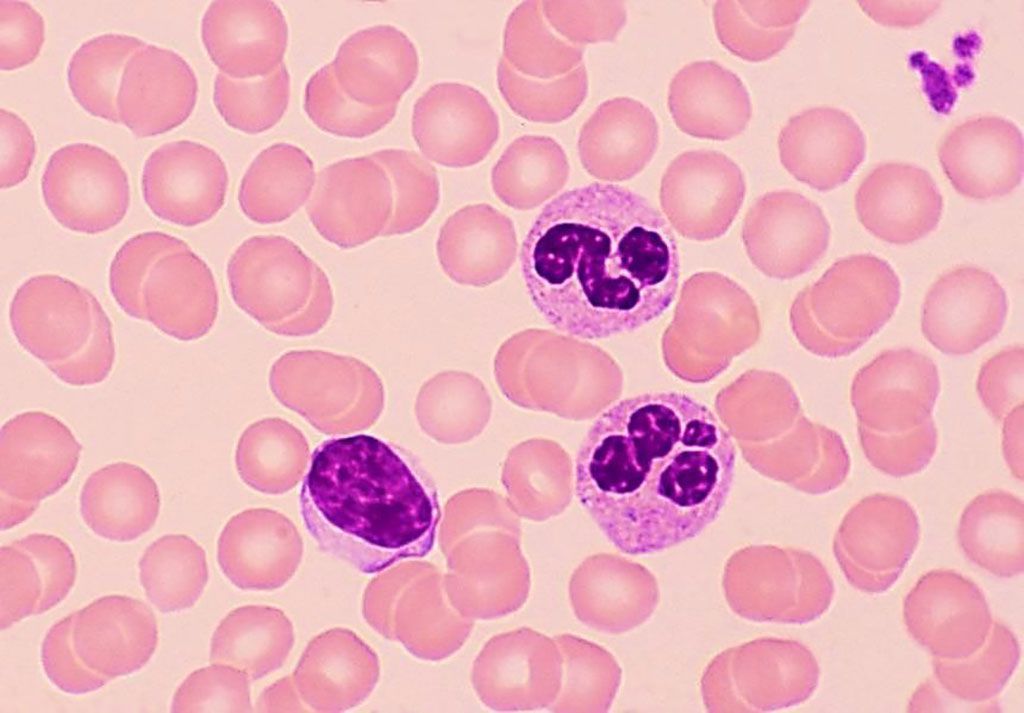
- Asociación entre la proporción de neutrófilos/linfocitos periféricos y la enfermedad hepática esteatósica asociada a disfunción metabólica en pacientes con diabetes tipo 2. Zhu N, Song Y, Zhang C, Wang K, Han J. Front Med (Lausana).2023; 10: 1294425.
Antecedentes: La enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD) y la diabetes tipo 2 con frecuencia coexisten, lo que impone una enorme carga médica. Un indicador MASLD conveniente y eficaz será beneficioso para el diagnóstico temprano de la enfermedad. En el laboratorio clínico, la proporción neutrófilos/linfocitos (NLR) es un marcador hematológico de fácil acceso. Este estudio se diseñó para determinar la relación entre el NLR y MASLD en pacientes con diabetes tipo 2.
Métodos: En el estudio retrospectivo se analizaron datos de 1.151 pacientes hospitalizados con diabetes tipo 2 sin infecciones, malignidades o enfermedades hematológicas que fueron reclutados entre 2016 y 2022. Los pacientes se estratificaron en terciles de NLR (población total: nivel alto de NLR > 2,18; nivel medio de NLR: 1,58-2,18; nivel bajo de NLR < 1,58), con estratificación adicional de subgrupos por sexo (hombres: nivel alto de NLR > 2,21; nivel medio de NLR : 1,60-2,21 y nivel NLR bajo< 1,60; mujeres: nivel NLR alto > 2,12; Después de ajustar por los factores de confusión (edad, sexo, peso, Glu, ALT y TG) asociados con MASLD, se obtuvieron el odds ratio (OR) y el correspondiente intervalo de confianza (IC) del 95% del NLR mediante el uso de un análisis de regresión logística binaria para verificar la correlación entre el NLR y MASLD.
Resultados: En comparación con los pacientes sin MASLD, los pacientes con MASLD tuvieron mayor peso, glucosa en sangre, insulina y péptido C, peor función hepática (ALT y GGT más altos), HDL más bajo (todos p < 0,05) y NLR más bajo (p < 0,001). ). La prevalencia de MASLD fue de 43,75% (nivel alto de NLR), 55,21% (nivel medio de NLR) y 52,22% (nivel bajo de NLR) (p < 0,05). En comparación con los del nivel alto de NLR, las OR ajustadas y los IC del 95 % de los niveles medio y bajo de NLR fueron 1,624 (IC del 95 %: 1,141-2,311) y 1,456 (IC del 95 %: 1,025-2,068), para todos los sujetos, mientras que fueron 1.640 (IC 95%: 1.000-2.689) y 1.685 (IC 95%: 1.026-2.766), para los hombres.
Conclusión: Un NLR bajo se asocia con un mayor riesgo de MASLD.
- ELA plasmática y Gal-3BP se diferencian tempranamente de la fibrosis hepática avanzada en pacientes con MASLD. Pérez Compte D, Etourneau L Hesse AM, Kraut A, Barthelon J, Sturm N, Borges H, Biennier S, Courçon M, de Saint Loup M, Mignot V, Costentin C, Burger T, Couté Y, Bruley C, Decaens T, Jaquinod M, Boursier J, Brun V. Biomark Res. 2024; 12(1):44.
Antecedentes: Se estima que la enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD, por sus siglas en inglés) afecta al 30% de la población mundial, y su prevalencia está aumentando junto con la obesidad. La fibrosis hepática está estrechamente relacionada con la mortalidad, lo que la convierte en el parámetro clínico más importante para MASLD. Actualmente se evalúa mediante biopsia hepática, un procedimiento invasivo que tiene algunas limitaciones. Por tanto, existe una necesidad urgente de un medio no invasivo confiable para diagnosticar etapas tempranas de MASLD.
Métodos: Se realizó un estudio de descubrimiento en 158 muestras de plasma de pacientes con MASLD caracterizados histológicamente utilizando proteómica cuantitativa basada en espectrometría de masas (EM). Se seleccionaron proteínas diferencialmente abundantes para su verificación mediante ELISA en la misma cohorte. Posteriormente fueron validados en una cohorte independiente de MASLD (n = 200).
Resultados: De las 72 proteínas diferencialmente abundantes entre pacientes con fibrosis temprana (F0-2) y avanzada (F3-4), seleccionamos la subunidad lábil ácida (ELA) del complejo proteico de unión al factor de crecimiento similar a la insulina y la proteína de unión a Galectina-3. (Gal-3BP) para estudio adicional. En nuestra cohorte de validación, se obtuvieron AUROC con IC del 95 % de 0,744 [0,673 - 0,816] y 0,735 [0,661 - 0,81] para ELA y Gal-3BP, respectivamente. La combinación de ALS y Gal-3BP mejoró la evaluación de la fibrosis hepática avanzada, dando un AUROC de 0,796 [0,731. 0,862]. La {ELA; El modelo Gal-3BP} superó los paneles de fibrosis clásicos en la predicción de la fibrosis hepática avanzada.
Conclusiones: Se necesitarán más investigaciones con cohortes complementarias para confirmar la utilidad de ALS y Gal-3BP individualmente y en combinación con otros biomarcadores para el diagnóstico de fibrosis hepática. Con la disponibilidad de ensayos ELISA, estos hallazgos podrían traducirse clínicamente rápidamente, proporcionando beneficios directos para los pacientes.
Bibliografía
En inglés
- Santoro S, Khalil M, Abdallah H, Farella I, Noto A, Dipalo GM, et al. Early and accurate diagnosis of steatotic liver by artificial intelligence (AI)-supported ultrasonography. Eur J Intern Med. 2024;125:57-66.
- Zsombor Z, Rónaszéki AD, Csongrády B, Stollmayer R, Budai BK, Folhoffer A, et al. Evaluation of Artificial Intelligence-Calculated Hepatorenal Index for Diagnosing Mild and Moderate Hepatic Steatosis in Non-Alcoholic Fatty Liver Disease. Medicina (Kaunas). 2023;59(3):469.
- Zahoor F, Saeed NU, Javed S, Sadiq HZ, Mand Khan F, Haider M, et al. Association of Metabolic Dysfunction-Associated Steatotic Liver Disease/Non-alcoholic Fatty Liver Disease With Type 2 Diabetes Mellitus: A Case-Control Study in a Tertiary Care Hospital in Pakistan. Cureus. 2023;15(10):e47240.
- Yanai H, Adachi H, Hakoshima M, Iida S, Katsuyama H. Metabolic-Dysfunction-Associated Steatotic Liver Disease-Its Pathophysiology, Association with Atherosclerosis and Cardiovascular Disease, and Treatments. Int J Mol Sci. 2023;24(20):15473.
En español
- Ma Duarte EL, Hugo Merino GA. Enfermedad hepática metabólica: revisión bibliográfica. Salud ConCienc. 2023;2(2):e53.
- Guerra Ruiz AR, Casals G, Iruzubieta P, Lalana M, Leis A, López RM, Crespo J, Morales-Ruiz M. Valoración bioquímica en la enfermedad hepática grasa asociada a la disfunción metabólica. Adv Lab Med. 2021;2(2):209–19.
